Le cuivre est un métal connu depuis la plus haute antiquité, (au début cependant seul le cuivre natif était utilisé). Il est donc évident que les écoulements suintants des gisements ou des mines ont été remarqués rapidement, surtout par la formation de cristallisations caractéristiques.
Il semble qu'il faille attendre, en Occident, la période d'Albert le Grand pour que les alchimistes en parlent sous les noms de couperose, vitriol bleu.
Ce produit naturel s'échappant jadis des mines, les chimistes le nomment Sulfate de Cuivre.
On retrouve encore dans la littérature de toutes les époques les dénominations suivantes : vitriol bleu (à cause de sa couleur), couperose bleue, sulfate de cuivre, sulfate cuivrique, sulfate cuivrique penta hydraté.
C'est ce dernier, de formule Cu SO4 + 5H2O qui fera l'objet de cet article.
Sa masse molaire est de 269,68 g/mol. Sa densité est de 2,29 g/cc.
Sa solubilité dans l'eau à 20° C est de 370 g/litre (elle triple à 80° C)
Il est soluble également dans la glycérine et le méthanol.
Il est insoluble dans l'éthanol et les autres alcools.
Le pH d'une solution de 50 g/litre dans l'eau à 20° C est compris entre 3,5 et 4,5.
En le chauffant, le sulfate perd son eau de cristallisation et devient blanc. (il reprend sa teinte bleue en se réhydratant).
Il se décompose vers 560° C.
Nota : Une variété géologique de cristaux, la Bonattite n'a que 3 molécules d'eau.
OBTENTION :
Les Anciens obtenaient ce sulfate par récupération des eaux d'écoulement des mines et évaporation naturelle, ou par chauffage. Par la suite, ils grillèrent en tas des mélanges de combustible et de minerais contenant des sulfures de cuivre, exemple la Chalcosine (ou chalcosite) de formule Cu2S ou des pyrites cuivreuses, exemple la Chalcopyrite de formule Cu2S, Fe2S3.
Nous pouvons griller, pour les oxyder, des chutes de cuivre, puis traiter cet oxyde à l'acide sulfurique. Cependant, il nous a semblé plus simple de partir de chutes de cuivre laminées très mince, ou à défaut de fils de cuivre très fins que l'on peut se procurer facilement chez les ferrailleurs. Nous disons "très fins", car du fil de 0,05 mm de diamètre présente une surface d'attaque à l'acide 20 fois plus importante, à poids égal, que du fil de 1 mm de diamètre.
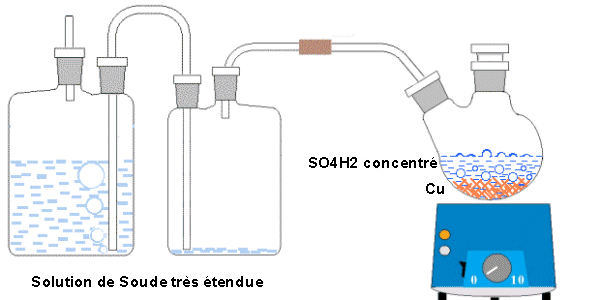
L'attaque des morceaux de fil se fait à chaud par de l'acide sulfurique concentré (l'esprit de Vitriol Romain d'Albert le Grand). Vous pouvez concentrer préalablement l'acide vendu en grande surface (il est parfaitement inutile d'utiliser une qualité Prolabo) ou admettre que dans un premier temps, il y aura à l'ébullition, évaporation de l'eau excédentaire avant que l'attaque ne se manifeste.
Ci-dessous, le montage théorique proposé. Les barboteurs sont garnis d'eau rendue basique par 10 % de lessive de soude (vendue en grandes surfaces) de façon à éviter que l'hydrogène généré par l'opération ne ressorte du montage accompagné de traces d'acide.
Il est suivi de deux exemples de montages pratiques.
|
 visiteur(s) sur le site.
visiteur(s) sur le site.